关于胆汁酸驱动新生儿肠道菌群的成熟研究。
健康宿主的肠道菌群代表了一个密集的微生物系统,并提供了一些代谢活性和免疫刺激性分子,这些分子共同促进宿主的代谢、组织发育和免疫系统的成熟,并保护其免受肠道致病菌的感染。人类肠道微生物群组成的变化与代谢和免疫疾病息息相关。因此,了解健康宿主中建立和维持有益微生物群组成的机制,尤其是婴儿早期的微生物定殖对于长期的微生物群组成以及免疫方面的影响至关重要。
目前很少有研究分析宿主介导的内源性物质的变化机制,如婴儿出生后早期微生物生态系统是否与遗传有关,是否与宿主的代谢有关等等,这些变化大多是宿主-微生物共同作用共同进化的结果。在本研究中,研究人员旨在通过组学的手段揭示婴儿早期发育过程中宿主肝脏代谢对肠道菌群的影响。
部分结果展示:1. 产后肠道菌群组成的变化
为了研究产后肠道微生物的发育情况,研究人员收集了出生后0小时、6小时、12小时、18小时、24小时以及1天、7天、14天、28天、56天的肠道内容物样本,通过16s rRNA进行分析。结果显示,出生后最初的24小时,小肠和结肠中细菌的丰富度和多样性均显著降低,仅Corynebacterium和 Mannheimia的丰度分别在6-18小时和24小时时达到峰值。出生后最初的微生物丰度降低可能表明出生时以及此后不久摄入细菌的瞬时传播,然而这些细菌无法永久的定居在肠道中(如Corynebacterium)。因此研究人员将研究的重点放在较晚的时间点。
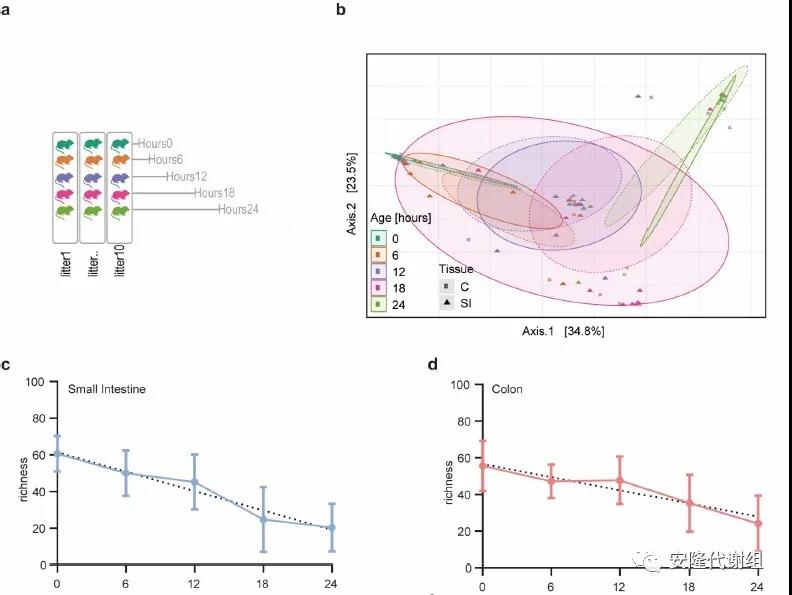
图、产后短时间内肠道菌群组成的变化
从第7天开始,小肠和结肠中的微生物丰度开始增加。值得注意的是,这一结果揭示了很大一部分源自环境(非母亲)来源的变形杆菌(结肠的78.2%和小肠OTU的73.2%)在出生后的早期阶段就为肠道微生物群的组成做出了重要的贡献。同时,放线菌、拟杆菌在整个研究阶段内持续存在,其中在结肠和小肠中分别占53.3-94.2%和45-86.5%。因此,早期变形杆菌在结肠中最为丰富,而小肠中变形杆菌和放线菌较为丰富。
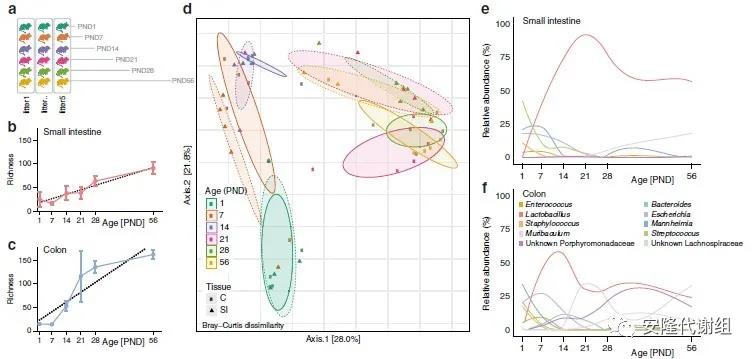
图、产后不同时间点肠道菌群的组成
2. 与微生物群相关的代谢变化
一般产后肠道的酶活性、肠道的吸收能力以及肝脏的代谢能力逐渐成熟,相关的代谢变化有助于细菌的定殖。研究人员对同一饲养条件下小鼠的肝脏代谢物进行了分析,发现在PND7和PND21、PND28和PND56之间存在与年龄显著相关的代谢差异。尤其是氨基酸、生物胺、酰基肉碱和一些甘油磷脂在这些时间点之间显着下降,这很可能是由于断奶期间饮食的改变所致。相反,断奶后胆汁酸的数量显着增加,尤其是在PND7与PND28以及PND7与PND56之间。
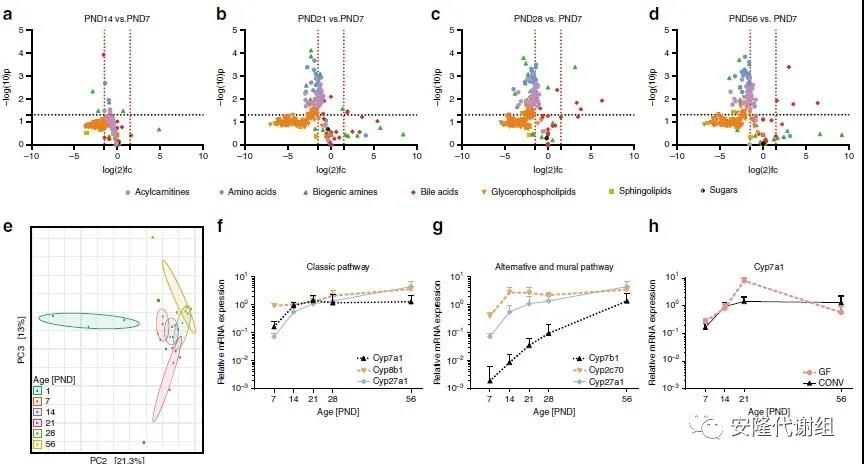
图、产后代谢的变化情况
3. 产后胆汁酸的合成、修饰和重吸收
与胆汁酸代谢相关的关键酶,如胆盐水解酶(BSH,KO1442)的预测基因丰度随着年龄的增长而增长,大约在PND 21-28时在小肠中达到最高水平。此外,与胆汁酸肝胆运输有关的蛋白质(例如Ntcp(Slc10A1),Abcb11和Abcb4)以及与Fxr-Fgf15-Fgfr4负反馈环调控蛋白有关的基因表达稳定增加,出生后直至PND 56为止在肝脏均观察到新胆酸的合成。细菌修饰的次级胆汁酸的浓度随年龄增长而增加,而初级胆汁酸的浓度则下降。因此,宿主的胆汁酸生物合成能力和肝胆运输系统的成熟与细菌胆汁酸代谢相关联,导致断奶后总胆汁酸池及其组成发生明显变化。然而,在出生后的小肠中主要存在的是结合型胆汁酸。
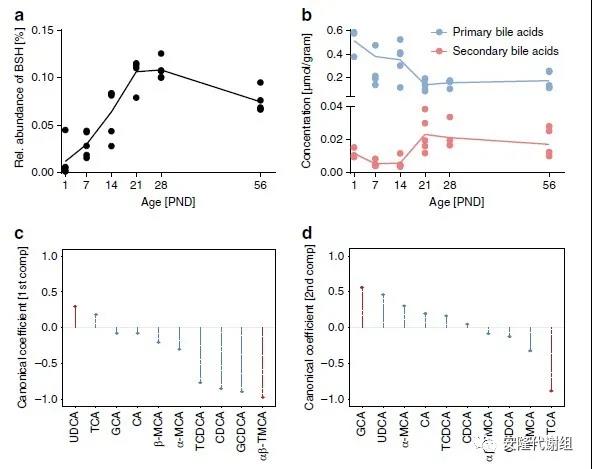
图、微生物群落成熟过程中的肝肠合作
4. 胆汁盐介导的新生儿肠道菌群的成熟
接下来,研究人员对新生小鼠口服食用了四个胆汁酸UDCA、GCA、βTMCA和TCA,并评估了它们对发育中的小肠微生物群的影响。在PND7-PND9之间连续三天,新生小鼠通过强饲法接受指定的胆汁酸以及PBS作为对照,在PND9确定了特定部位的小肠微生物群组成。PCoA揭示了TCA和βTMCA使得微生物群组成向成年鼠的微生物群转变。同时,TCA和βTMCA的食用显着增加了小肠微生物群的丰富度,并缩短了与成年鼠菌群组成的距离。相比之下,GCA和UDCA对细菌丰富度没有影响。
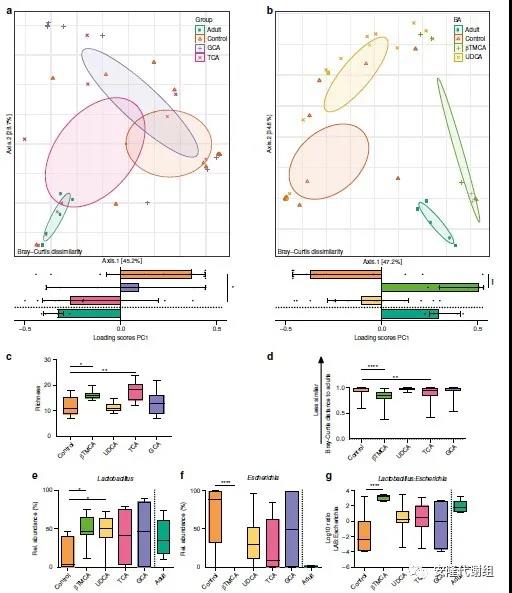
图、新生小鼠口服胆汁酸可加速微生物的成熟
小结:
本研究发现胆汁酸是驱动产后小鼠肠道微生物群做成的关键因素,产后胆汁酸合成的增加和肝肠循环的成熟可能有助于塑造早期的肠道菌群。新生儿肝脏能够产生和分泌的胆汁酸会进入小肠,产后共轭胆汁酸占主导地位,断奶后以小肠中浓度最高,这些微生物组成可能对新生儿粘膜免疫系统的成熟与发育起着至关重要的作用。另外,口服两种共轭胆汁酸均增强了新生儿小肠微生物群的丰富性,使其与成人的更为相似。本研究为研究新生儿早期肠道菌群的定殖提供策略及思路,在生命早期如何平衡肠道菌群,使得微生物在体内达到平衡,对于新生儿的健康具有重要贡献。

 微信公众号
微信公众号